本邦にて2019年12月~2021年7月の間に、53施設で患者500名を登録した、使用成績調査です。
本稿ではその3年までの成績を報告します。
デザイン
前方視、多施設、単群調査。日本国内の53施設が参加し、2019年12月から2021年7月までの間に500名の患者を登録した
適格基準
PFOが関与する潜因性脳梗塞患者で、Amplatzer™ PFO Occluderをインプラントされた全患者
フォローアップ
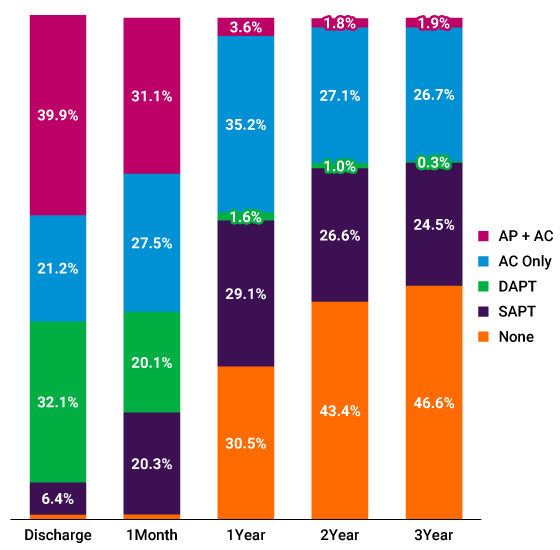
ベースライン、手技時、退院時、術後30日・1年・2年・3年時点
主要評価項目(各施設による評価)
- 早期: 30日時点、事前に定められたデバイスもしくは/かつ手技関連の有害事象*
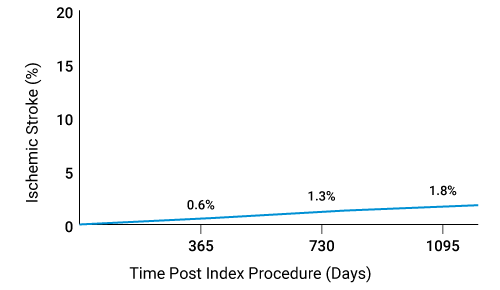
- 長期:30日~3年時点、肺塞栓症(PE)・深部静脈血栓症(DVT)・心房細動(AF)・虚血性脳卒中の発生率
* 有害事象に含まれるイベントは次の通り:心房細動(AF)、肺塞栓症(PE)、深部静脈血栓症(DVT)、デバイス血栓、エロージョン、虚血性/出血性脳卒中、輸血/外科的あるいは血管内治療介入を要する出血、外科的治療介入を要するアクセスサイトの合併症、致死的なデバイス/手技関連の有害事象